永利官网
Circulation Research | 周菁课题组与合作者发现基质刚度通过盘状结构域受体1(DDR1)的“液-液”相分离机制抑制Hippo通路
动脉硬化在慢性肾病患者中普遍存在,其发生率和严重程度与心血管危险因素密切相关,包括年龄、高血压、糖尿病和高脂血症等。细胞外基质(ECM)刚度可影响血管平滑肌细胞(VSMCs)的表型和行为。ECM硬化会导致VSMC过度增殖、迁移,并从收缩表型向合成表型转化。然而,细胞是如何感知ECM刚度的改变,并将力学信号转化成生物学信号,这一问题仍有待深入研究。
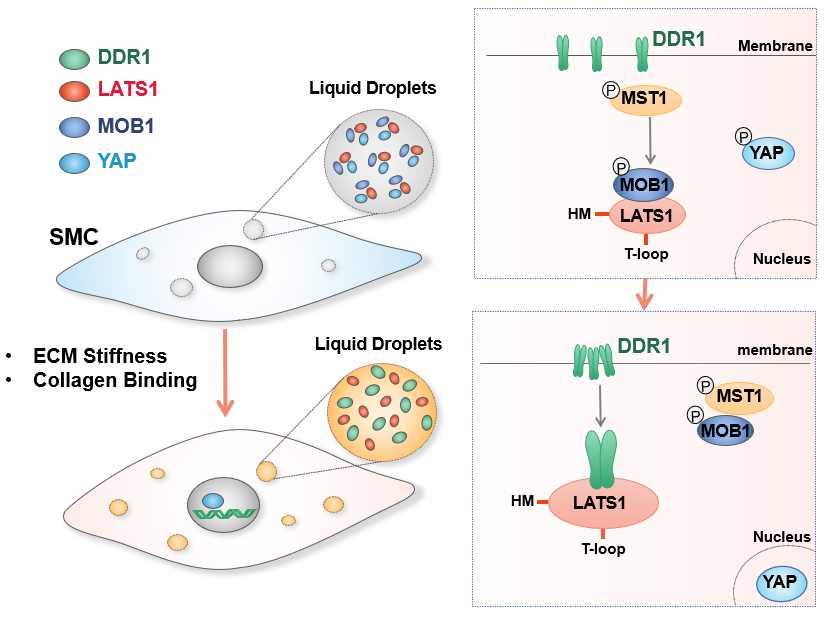
2022年12月8日,北京大学医学部yl9193永利生理学与病理生理学系周菁课题组与天津医科大学yl9193永利王晓虹教授等合作在Circulation Research杂志上在线发表了题为LLPS of DDR1 Counteracts the Hippo Pathway to Orchestrate Arterial Stiffening的研究论文。该研究发现ECM刚度/胶原刺激下的DDR1发生了“液-液”相分离(LLPS),并与Hippo通路的核心激酶LATS1形成共凝聚物,从而抑制了LATS1对YAP的磷酸化,导致YAP的入核和下游靶基因的激活。

此项研究中,研究者通过在体外采用不同基质刚度的水凝胶模型,体内采用5/6肾切诱导的慢性血管硬化模型,证实了DDR1可以介导血管刚度诱导的YAP活化。通过活细胞成像,荧光漂白恢复,体外相分离,免疫共沉淀以及GST-pull down等技术,此研究揭示了DDR1在胶原或基质刚度刺激下与LATS1发生共同相分离以抑制Hippo通路激活的分子机制。活化的DDR1与LATS1形成共凝聚物,竞争性地抑制了MOB1-LATS1的结合,从而导致LATS1去磷酸化和YAP活化。这是首个证明LLPS在介导血管疾病中作用的研究,证明了DDR1-LATS1-YAP轴在VSMC机械信号转导中的中心作用,并提供了抗动脉硬化的潜在治疗靶点。
图:基质刚度诱导VSMCs中DDR1-LATS1共凝聚物的形成和YAP入核
yl9193永利博士生刘佳钰和王谨为本文的共同第一作者。yl9193永利周菁教授和天津医科大王晓虹教授为为本文的共同通讯作者。本研究得到了国家自然科学基金重大研究计划集成项目、创新研究群体和面上项目等经费支持。周菁课题组长期从事血管稳态和疾病的力学调控机制研究,研究结果发表在在Proc. Nat. Acad. Sci. USA、Bioactive Materials、Advanced Science、Circ Res.等学术期刊。
全文链接:https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.122.322113